世界阿尔茨海默病日 | 脑磁图将为AD的早期诊断和精准治疗提供新的可能(上)
“爸,该吃饭了。”
“你是谁?”
......
阿尔茨海默病俗称老年痴呆,遗忘对阿尔茨海默病人来说是最寻常不过的事情,仿佛脑海中有一个记忆橡皮擦,让他们逐渐失去过去的记忆。除此之外,生活能力下降、性格改变等多种问题也伴随着阿尔茨海默病人。
9月21日是世界阿尔茨海默病日,根据国际阿尔茨海默病协会的报告显示,每隔3秒,全世界就会多一位阿尔茨海默病患者。关爱老年人群、关爱阿尔茨海默病人,早发现、早干预是最有效的手段之一。
脑磁图作为一种高时空分辨率、无创伤、无辐射的新兴脑功能影像技术,对阿尔茨海默病的早期诊断有着重要意义。昆迈医疗作为自主化高端脑功能影像设备引领者,也在不断探寻脑磁技术在阿尔茨海默病等神经系统疾病中的应用可能。
受限于篇幅,本次我们将用上、下两篇文章来探讨脑磁图在阿尔茨海默病早期诊断和精准诊疗的应用。
什么是阿尔茨海默病(AD)?
阿尔茨海默病 (AD) 是一种逐渐发展的、导致大脑功能损害的神经退行性疾病,是最常见的痴呆症,患者会逐渐出现记忆力减退、认知能力下降、语言能力衰退等症状。目前影响全球超过 3500 万人,65岁以上老年人阿尔茨海默病患病率在发达国家约为4%~8%,我国约为3%~7%,女性高于男性。年龄是 AD 的最大风险因素,随着全球预期寿命的延长,预计到 2050 年,AD 患者人数将达到 8700 万[1],极大地影响了老年人的健康生活水平,也给家庭和社会造成了沉重的负担。
虽然具体原因仍在研究中,但主要认为突触受损与认知功能下降的相关性最强。而突触受损则主要与以下两种蛋白质异常积累有关:
· β淀粉样蛋白(Aβ):在大脑中形成斑块。
· 超微结构蛋白tau:形成纤维缠结,导致神经细胞死亡[2]。

AD目前的临床诊疗难点
1.早期诊断
由于AD早期只有神经病理学的改变,而缺少显著的临床症状表现,因此早期AD难以准确识别和鉴定,很容易被忽视。AD 现在通常被认为是一个无缝的连续体,包含三个主要阶段:“临床前”或症状前阶段,持续十多年,在此期间个体无症状,但存在AD神经病理学相关改变;“前驱”阶段,在此阶段,个体至少在一个认知领域受损,但保持良好的功能;以及更常见的“痴呆”阶段,其中多个认知领域受到影响,并伴有日常功能下降。
此外,在早期AD人群中进行试验设计也十分困难。需要准确的血浆测量、新的招募方法、敏感的认知工具和自我报告结果。这也导致在开发AD早期诊断工具和神经标志物等方面难以取得突破性进展。
2.分期和预测
除了根据症状对 AD 进行临床分期之外,现在还可以使用 ATN 框架根据病理学对患者进行分期(见下图)。“A”指淀粉样蛋白病理学,“T”指 tau 病理学,“N”指神经退变。该框架正在应用于整个 AD 病程,包括其临床前阶段,且已证明该框架有助于提供准确的诊断和预后。但由于个体之间的疾病进展速率存在很大差异,因此ATN框架的预测能力并不完善。此外,该框架中生物标志物的选择以及确定为阳性的具体阈值也有待进一步研究和讨论。临床中缺乏对AD分期和预测的定量指标和有效手段。
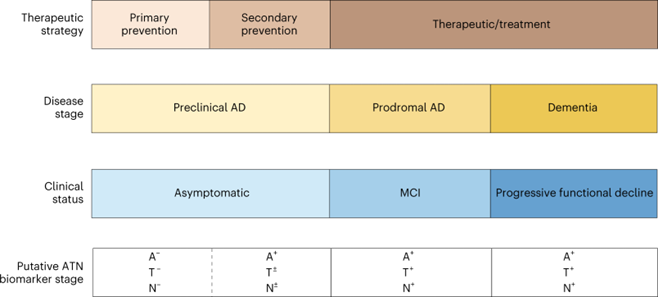
生物标志物与 ATN 框架[3]
-
早期诊断:早期症状可能非常轻微,容易被忽视。
-
病因不明:尽管有多种理论,但至今仍不确定AD的确切原因。
-
没有治愈方法:目前的治疗方法主要是缓解症状,不能阻止疾病进展。
-
病程预测:AD进展因人而异,目前缺乏准确的预测手段。
3. 治疗方法
目前还没有治愈AD的方法。现有的治疗方法主要集中在缓解症状,改善生活质量,以及尽可能地延缓疾病进展。目前,关于治疗AD的临床试验开展也较为困难,招募和保留多元化的试验参与者现在是开发下一代AD治疗方法的最大障碍。治疗的改善,极大地依赖诊断,分期和预测手段的改进。
总体而言,AD的诊断缺乏早期敏感性标志物,而临床开发工作也由于入组问题难以突破,形成了“先有鸡还是先有蛋”的问题困局;分期和预测难以形成定量的指标,个体化差异大;在治疗方面,招募患者也依然是难点,依赖于诊断和分期手段改进。
AD诊疗所面临的困局亟待解决,脑磁图(MEG)可以在体外以超高的时间分辨率和空间分辨率实时探测大脑的神经元活动,在AD的早期诊断和精准治疗中有着巨大的应用潜力。
昆迈医疗将在下篇文章中带您了解什么是脑磁图,以及脑磁图在阿尔茨海默病领域的应用。
参考文献:
[1] WHO. Global action plan on the public health response to dementia 2017–2025 (WHO, 2017).
[2] Tzioras, M., McGeachan, R. I., Durrant, C. S., & Spires-Jones, T. L. (2023). Synaptic degeneration in Alzheimer disease. Nature Reviews Neurology, 19(1), 19-38.
[3] Rafii, M. S., & Aisen, P. S. (2023). Detection and treatment of Alzheimer’s disease in its preclinical stage. Nature Aging, 3(5), 520-531.

